氯化铝
氯化鋁,或三氯化铝,化學式為,是氯和鋁的化合物。氯化鋁熔點、沸點都很低,且會昇華,為有離子性的共價化合物。熔化的氯化鋁不易導電[1],和大多數含鹵素離子的鹽類(如氯化鈉)不同。
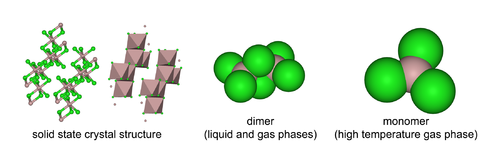
采取结构,为Al3+立方最密堆积层状结构,[2] 而中Al3+却占Br−最密堆积框架的相邻四面体间隙。熔融時生成可揮發的,含有兩個三中心四電子氯橋鍵,更高温度下Al2Cl6二聚體則離解生成平面三角形,與結構類似。
氯化鋁是很常用的路易斯酸。在化學工業,它常是傅-克反應的催化劑。它亦用於烴的聚合和异构化反应中。
鋁亦可以生成一氯化鋁(),但這种化合物很不穩定,只能以氣態的形式出現。
工業上,它經鋁土礦加工,由鋁和氯之間的放熱反應所製。
制备
無水氯化鋁可由氧化鋁和碳的混合物與氯氣反應得到:[3]
也可由鋁和鹽酸的混合物得到:
化學性質
氯化鋁是強路易斯酸, 可和路易斯鹼作用產生化合物,甚至也可和二苯甲酮和均三甲苯之類的弱路易斯鹼作用。[4]若有氯離子存在,氯化鋁會生成(四)氯鋁酸根離子AlCl4−:
- AlCl3(aq) + Cl−(aq) Template:Unicode AlCl4−(aq)
在水中,氯化鋁會部分水解,形成氯化氫气体或H3O+離子。其水溶液和其他含鋁物质的溶液相同,含有水合铝离子,跟適當份量的氫氧化鈉反應可生成氫氧化鋁沉淀:[5]
- AlCl3(aq) + 3 NaOH(aq) → Al(OH)3(s) + 3NaCl(aq)
- AlCl3(aq) + 3 H2O → AlO2-+ 3HCl + H3O+Template:Cn
用途
氯化鋁主要用在傅-克反应[4] 中,例如以苯和光氣為原料制備蒽醌,应用于染整工業中。[1] 在廣義的傅-克反应中,醯氯或鹵代烷和芳香族物質的反應式如下:[4]
苯及其衍生物在發生上述反應時,主產物是對位的異構物。相比較下,烷基化反應涉及的問題較多,不如酰基化反應應用廣泛。無論是哪種反應,氯化鋁和其他原料和儀器都必須是中等乾燥的,少量的水有助於反應進行。
由於氯化鋁可與反應產物配位,因此應用在傅克反應時,它的用量必須與反應物相同,而非「催化量」。反應後的氯化鋁很難回收,會產生大量的腐蝕性廢料。為了達到綠色化學的要求,化學家開始使用三氟化釔或三氟化鏑來替代氯化鋁,減少污染。
氯化鋁也常用來將醛基加在苯環上,如加特曼-科赫反應用一氧化碳、氯化氫、氯化鋁及氯化亞銅為催化劑[6]
氯化铝在有机化学中有很广泛的应用。[7] 它可以催化Ene反應,比如3-丁烯-2-酮(甲基乙烯基甲酮)与香芹酮加成:[8]
氯化鋁也常用在烃类聚合反应和异构化反应中,重要的例子包括[1] 工业上乙苯的生产。乙苯可用于进一步制备苯乙烯、聚苯乙烯以及用作清洁剂的十二烷基苯。
芳烃存在下,氯化铝与铝混合可用于合成二(芳烃)金属配合物。例如,二苯铬就是通过特定金属卤化物经由Fischer-Hafner合成制备的。
低濃度的碱式氯化铝常是防汗药的成分之一,而多汗症患者在使用时浓度会高些(12%或更高)。
氯化铝和氯化钠不同,其化学键的構成大部分是共价键,而离子键的佔比極低,因此熔融態的氯化鋁不易電離,且電離產生的Cl-會和氯化鋁分子結合生成更穩定的四氯合鋁酸根離子AlCl4−;並且氯化鋁在180 °C(356 °F)以上的溫度下會升华成為氣體;因此在工業上不會通過電解氯化鋁的方式量產金屬鋁。但是在熔融態的氯化鋁添加氯化鈉、無水氯化钙和少量的氯化锂,增强氯化铝分子的电离效率,添加氯酸钾阻止氯化铝的升华;用此方法可以电解制备高纯度的金属铝[9][10]。
注意事項
無水氯化鋁會和鹼劇烈反應,因此需妥善處理。含結晶水的氯化鋁較無此問題。
如果吸入無水氯化鋁或接觸眼睛和皮膚會造成刺激。
參考文獻
Template:Reflist Template:Portal Template:铝化合物 Template:氯化物 Template:Authority control
- ↑ 1.0 1.1 1.2 N. N. Greenwood, A. Earnshaw, Chemistry of the Elements, Pergamon Press, Oxford, United Kingdom, 1984.
- ↑ A. F. Wells, Structural Inorganic Chemistry, Oxford Press, Oxford, United Kingdom, 1984.
- ↑ Stover, Norman M.; Constantinescu, Clinton (1936). THE REACTION ALUMINIUM OXIDE–CARBON–CHLORINE. Canadian Journal of Research, 14b(9), 328–335. Template:Doi
- ↑ 4.0 4.1 4.2 G. A. Olah (ed.), Friedel-Crafts and Related Reactions, Vol. 1, Interscience, New York, 1963.
- ↑ Template:Cite web
- ↑ L. G. Wade, Organic Chemistry, 5th edition, Prentice Hall, Upper Saddle River, New Jersey, United States, 2003.
- ↑ P. Galatsis, in: Handbook of Reagents for Organic Synthesis: Acidic and Basic Reagents, (H. J. Reich, J. H. Rigby, eds.), pp12-15, Wiley, New York, 1999.
- ↑ B. B. Snider, Accounts of Chemical Research 13, 426 (1980).
- ↑ Template:Cite web
- ↑ Template:Cite web